Biotechnologies et santé: Contexte et historique


Il y a un siècle que l'industrie pharmaceutique est une véritable production industrielle, c'est à dire une production à moindre coût de grande quantité de petites molécules de qualité constante. Cette industrie est pilotée par des chimistes.
 Pour en savoir plus cliquez sur l'image
Pour en savoir plus cliquez sur l'image
C'est la production de la pénicilline en grande quantité qui a fait "exploser" l'industrie pharmaceutique. En France, compte tenu des enjeux à l'époque il a été envisagé une production nationalisée c'est à dire de créer un équivalent du CEA sur les antiobiotiques. Ce projet fut abandonné et la production laissée aux industriels.
 Pour en savoir plus cliquez sur l'image
Pour en savoir plus cliquez sur l'image
Les molécules trop complexes, comme par exemple les hormones, ne peuvent pas être synthétisées industriellement par une approche purement chimique. Elles sont produites dans des installations de fermentation industrielle par des micro-organismes ou cellules de mammifères OGM. L’insuline a été la première hormone OGM (commercialisée en 1982 par Eli Lilly). La liste s'est allongée depuis avec par exemple les interférons, l’hormone de croissance ou l'EPO. Il faut citer aussi la commercialisation en 1986 d’un vaccin contre l’hépatite B produit par génie génétique.
Sanofi fut la seule société pharmaceutique française à prendre le tournant du génie génétique.Ceci est lié au fait que son dirigeant venait de l’Institut Pasteur, alors que tous les autres groupes continuaient à être dirigés par des chimistes.
 Pour en savoir plus cliquez sur l'image
Pour en savoir plus cliquez sur l'image
C’est en 1975 que Köhler et Milstein (Grande-Bretagne) mirent au point une nouvelle technique, permettant d’obtenir des quantités illimitées d’anticorps extrêmement spécifiques, ne reconnaissant qu’un seul déterminant antigénique : les anticorps monoclonaux.
Cette invention modifia profondément le diagnostic médical. 
Les principaux fabricants de réactifs pour les tests immunologiques, comme Abbott aux USA, Behring et Boehringer-Mannheim en Allemagne, Amersham en Grande-Bretagne, Serono en Italie, CEA/Oris, BioMérieux et Diagnostics Pasteur en France, intégraient très largement les anticorps monoclonaux à leurs réactifs. De nouvelles sociétés spécialisées dans la fabrication d’anticorps monoclonaux et de kits de diagnostic furent créées à l’époque, avec Hybritech aux USA, Celltech en Grande-Bretagne. En France, trois sociétés (Immunotech – 1982, Clonatec – 1984, Transia – 1984) proposent aux laboratoires d’analyse un grand choix de kits diagnostics à base d’anticorps monoclonaux.
On entre ici dans un monde nouveau qui est diamétralement opposé à la production indutrielle telle qu'elle est décrite ci-dessus. On passe d'une production de masse fournissant un médicament à bas prix adapté au plus grand nombre à une pharmacie de type "chirurgicale". Le produit crée pour un malade (une culture de cellules génétiquement modifiées par exemple) ne sera pas valable pour un autre malade. Ce qui est reproductible c'est le savoir faire mais le produit n'est pas réutilisable. La conséquence est un coût très élevé des traitements .
La présentation des tendances actuelles des biotechnologies est compliquée car l’avenir ne dépend pas seulement des progrès de la science, il est fortement conditionné par l’attitude de la société. Pour s’en convaincre, il suffit de voir les troubles provoqués par l’industrialisation du vivant, dans le secteur agro-alimentaire tout d’abord (OGM, farines animales), mais aussi pour les tests génétiques (au bénéfice de qui sont-ils réalisés ?) ou l’utilisation d’embryons humains à des fins thérapeutiques.
On isole depuis longtemps diverses protéines thérapeutiques du sang, de l’urine et de tissus animaux ou humains. Mais ceci ne va pas sans de gros risques de transmission virale, tuant le patient au lieu de le guérir (sang contaminé, hormone de croissance contaminée, etc.). Seul le génie génétique garantit la fourniture de protéines humaines pures.
Les plantes et les animaux génétiquement modifiés peuvent produire des molécules thérapeutiques ou des vaccins. Les recherches phares portent sur les produits sanguins (tabac produisant de l’hémoglobine humaine, tabac et pomme de terre produisant de l’albumine), les vaccins (banane vaccin prévenant les gastro-entérites dans les pays en développement) et les protéines humaines (brebis produisant de l’antitrypsine alpha). Cependant il n’existe pas encore d’animaux ou de plantes transgéniques assurant une production industrielle. L’obtention d’un animal transgénique produisant une quantité substantielle de la molécule intéressante est extrêmement aléatoire, ce qui justifie qu’on multiplie les meilleurs animaux par clonage (comme la brebis Dolly).
 Le professeur Ian Wilmut et sa brebis Dolly [Keystone]
Le professeur Ian Wilmut et sa brebis Dolly [Keystone]
Un exemple particulièrement intéressant est la production d’érythropoïétine, une hormone qui n’est pas produite en quantité suffisante dans l’organisme pour pouvoir être isolée. Comme l’érythropoïétine déclenche la fabrication de globules rouges, elle est administrée aux malades souffrant de certaines formes d’anémie (de 100 à 150 000 personnes au monde) et les sportifs l’ont adoptée pour lutter contre la fatigue. Elle est produite industriellement par des cellules transgénique de Hamster chinois cultivées en fermenteur. C’est actuellement la protéine humaine issue du génie génétique la plus vendue au monde.
En 1993, le Téléthon  a vulgarisé la thérapie génique en en faisant, dans l’esprit du public français, la méthode thérapeutique la plus prometteuse. Malgré une activité intense des grands groupes pharmaceutiques et des jeunes entreprises de biotechnologie, les problèmes sont loin d’être résolus, tant pour la création de vecteurs capables de porter le gène intéressant dans la bonne cellule, que pour le contrôle de la multiplication des cellules transformées. Les deux tiers des essais cliniques de thérapie génique concernent actuellement le traitement de certains cancers car le but visé est apparemment simple : il suffit qu’une expression transitoire du transgène provoque la mort de la cellule cancéreuse. Malgré cela, il n’y a que peu de traitements suffisamment avancés pour faire l’objet d’essais sur des malades.
a vulgarisé la thérapie génique en en faisant, dans l’esprit du public français, la méthode thérapeutique la plus prometteuse. Malgré une activité intense des grands groupes pharmaceutiques et des jeunes entreprises de biotechnologie, les problèmes sont loin d’être résolus, tant pour la création de vecteurs capables de porter le gène intéressant dans la bonne cellule, que pour le contrôle de la multiplication des cellules transformées. Les deux tiers des essais cliniques de thérapie génique concernent actuellement le traitement de certains cancers car le but visé est apparemment simple : il suffit qu’une expression transitoire du transgène provoque la mort de la cellule cancéreuse. Malgré cela, il n’y a que peu de traitements suffisamment avancés pour faire l’objet d’essais sur des malades.
Les incertitudes scientifiques sont telles qu’il est aujourd’hui difficile d’apprécier la place qu’occupera la thérapie génique dans une dizaine d’année. La prudence s’impose ; les USA n’avaient-ils pas déclaré la guerre au cancer au début des années 1970, programmant la disparition de la maladie avant la fin du XX è siècle ?
L’invention de la PCR par Mullis provoqua une révolution dans le monde des tests diagnostics puisqu’elle permet de repérer un seul fragment d’une molécule d’ADN donnée au milieu d’un mélange. Les applications sont innombrables, allant de l’identification des pathogènes à la résolution de problèmes de police judiciaire, en passant par les tests génétiques permettant de déceler une prédisposition à telle ou telle maladie. Dans le monde entier, de très nombreuses petites sociétés vivent de ce marché, chacune d’elles payant des royalties à Hoffmann-Laroche pour l’utilisation de la PCR.
 Machine à PCR
Machine à PCR  Résultats PCR
Résultats PCR
On ne peut pas parler d'industrie pharmaceutique et de biotechnologies rouges sans aborder les aspects financiers de ce marché.

Les deux principales phases du cycle de vie d'un médicament sont:
Le développement coûte deux fois plus cher que la recherche proprement dite.
Globalement lorsqu' un nouveau médicament arrive sur le marché, il a couté en moyenne 7 milliards si on tient compte de l'amortissement des innombrables essais infructueux. L'objectif de la société qui le commercialise est de rembourser cette somme avant que le produit ne tombe dans le domaine public. Sachant que les brevets couvrent généralement la commercialisation du produit pendant 7 ans (voir la figure ci-dessus), il faut donc vendre le médicament à hauteur d'un milliard par an ce qui donne une idée des enjeux.

Ce qui est important de constater dans ce tableau c'est qu'en moyenne les bénéfices des compagnies pharmaceutiques représentent environ 20% des ventes ce qui est comparable aux bénéfices dans secteur informatique, dans l'industrie pétrolière ou dans la production de boissons . Le secteur bancaire ou minier se situe bien au dessus de cette moyenne. D'un point de vue industriel, et contrairement aux idées reçues, on peut dire que les bénéfices du secteur pharmaceutique sont "normaux". Les industries pharmaceutiques sont rentables certes mais sans excès de profit en leur faveur.
Il faut noter que si on diminuait de 20% les prix des médicaments, cela n'éviterait pas que les nouveaux médicaments soient très chers. Et cela ne supprimerait pas pour autant le déficit de la Sécurité sociale...
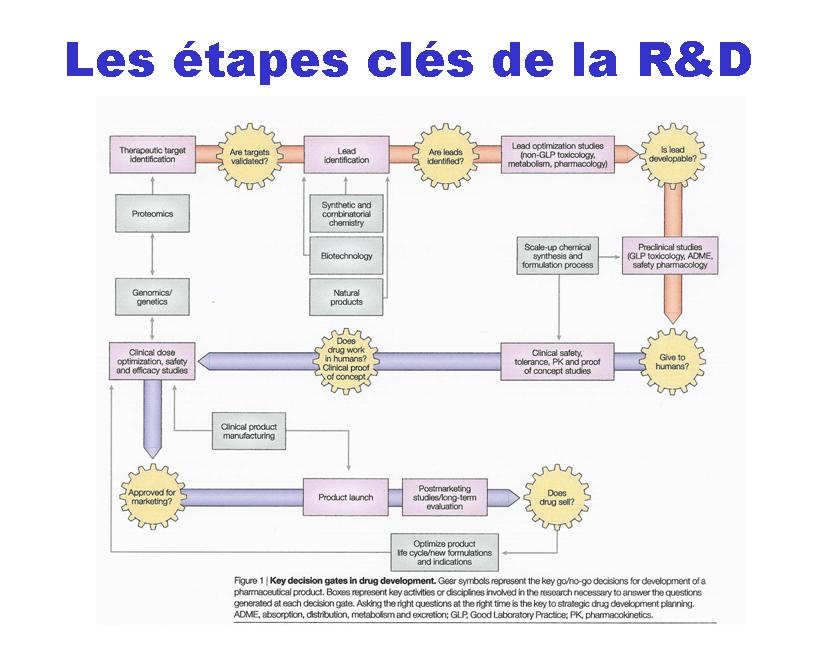


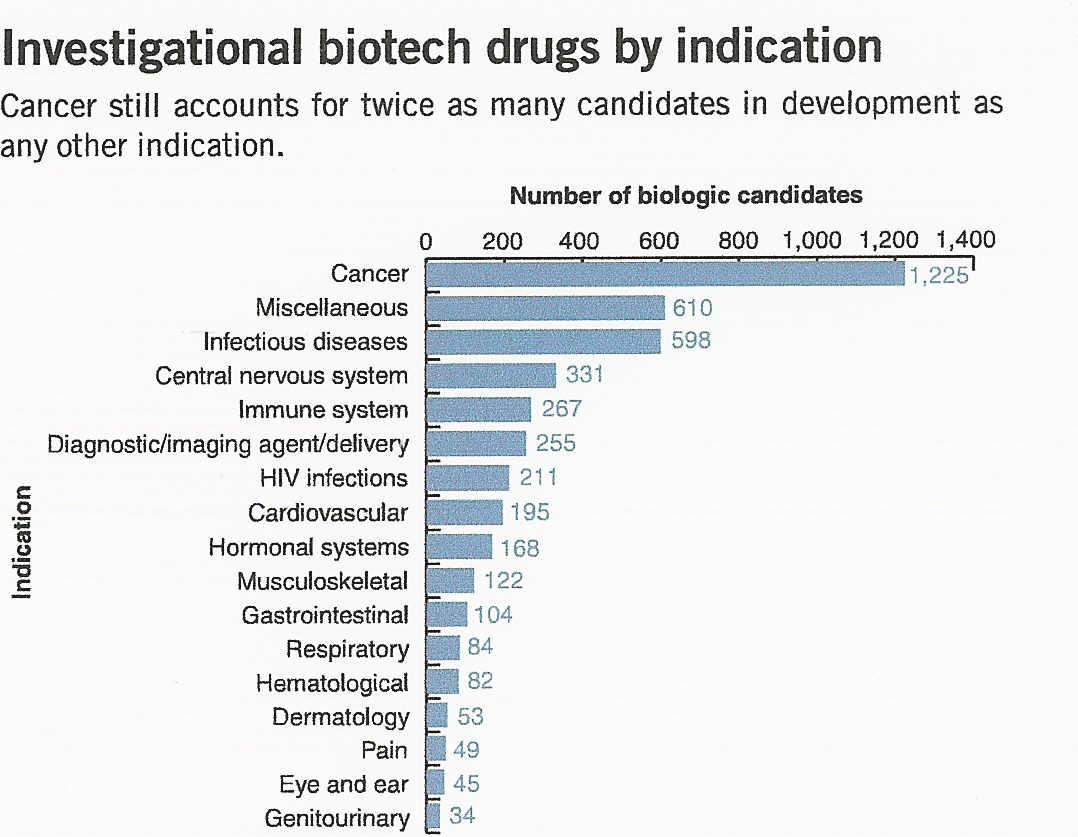
L'industrie pharamceutique est le secteur qui investit le plus en R&D. Les efforts portent sur les maladies pour lesquelles on est encore loin d'avoir trouver une solution : anticancéreux, anti-infectieux ...

On notera deux points importants dans ce tableau. La première entreprise mondiale du point de vue investissement en R&D est une entreprise du secteur pharmaceutique (Pfizer, USA) et, dans le classement mondial, la première entreprise française à apparaitre vient aussi du secteur pharmaceutique puisqu'il s'agit de Sanofi Aventis.
Plus des deux- tiers des investissements de R&D de l'industrie pharmaceutique concernent la chimie et le reste des biotechnologies ( cliquez ici pour voir l'évolution des investissements depuis 1998).
L'industrie pharmaceutique a tendance à acheter "clé en main" des molécules innovantes créées par des petites entreprises, surtout en biotechnologies. Le grand groupe pharmaceutique évite les aléas de la R&D et la petite entreprise a accès à un réseau de distribution international. La logique étant purement financière, le grand groupe essaie de racheter la nouvelle molécule le plus tardivement possible afin de minimiser les coûts avant commercialisation (illustration).

L'industrie pharmaceutique se heurte actuellement à une grande difficulté pour trouver de nouvelles molécules. Bien souvent, les nouveautés annoncées ne sont que des modifications de médicaments déjà existants sous une autre forme. Cette absence de nouveauté explique l'âpreté de la guerre que se mène les compagnies au travers des brevets et des génériques. Sans nouveauté on tend à s'accrocher et à proteger ce que l'on possède. On est alors dans une logique purement financière et non plus industrielle. Pour mémoire, l'industrie pharmaceutique dépose dix fois moins de brevets à R&D équivalente que les telecoms ou le secteur automobile.
Dans les cas graves, il existe des garde-fous contre un excès de protectionnisme des groupes pharmaceutiques. Lorsque l'intérêt public est en jeu (par exemple pour les médicaments anti-VIH), un tribunal ou l'Organisation Mondiale de la Santé (OMS) peuvent obliger la compagnie qui possède le brevet à vendre des licences à d'autres compagnie afin qu'elles produisent à leur tour ce médicament. Dans ce cas, un appel d'offre international est émis et chaque pays où au moins une compagnie a pris une licence peut produire de façon autonome le médicament concerné.

Pourquoi la situation dans l'industrie pharmaceutique apparait-elle comme crispée face à l'émergence des médicaments génériques? Il faut savoir que sur les 10 médicaments les plus vendus en 2004, seuls 2 resteront sous brevet en 2011! Or, pour les sociétés leaders actuellement sur le marché, leur succès porte sur 2 ou 3 produits qui vont donc tomber inévitablement à court terme dans le domaine public. Cette situation combinée avec le peu de dépôt de nouveaux brevets explique les réactions face aux médicaments génériques.

© Université
de TOURS - GÉNET
Document modifié le
20 mai, 2010